Comment faire Aspirine - Acide acétylsalicylique

L'aspirine est l'acide acétylsalicylique. Stephen Swintek / Getty Images
L'aspirine est le plus largement utilisé over-the-counter médicaments dans le monde. Le comprimé contient en moyenne environ 325 milligrammes de l'ingrédient actif acide acétylsalicylique avec un matériau liant inerte tel que l'amidon. L'aspirine est utilisé pour soulager la douleur, réduire l'inflammation, et faire baisser la fièvre. Aspirine était à l'origine dérivé en faisant bouillir l'écorce de l'arbre de saule blanc. Bien que la salicine dans l'écorce de saule a des propriétés analgésiques, l'acide salicylique purifié était amer et irritant lorsqu'ils sont pris par voie orale. L'acide salicylique a été neutralisé avec du sodium pour produire le salicylate de sodium, ce qui était mieux au goût mais toujours irrité l'estomac. L'acide salicylique peut être modifié pour produire phénylsalicylate, qui a été meilleur goût et moins irritant, mais libéré le phénol de substance toxique lorsqu'il est métabolisé. Felix Hoffman et Arthur Eichengrün première synthèse du principe actif dans l'aspirine, l'acide acétylsalicylique, en 1893.
Dans cet exercice de laboratoire, vous pouvez préparer l'aspirine (acide acétylsalicylique) à partir d'acide salicylique et de l'anhydride acétique en utilisant la réaction suivante:
Continuez à 2 sur 5 ci-dessous.
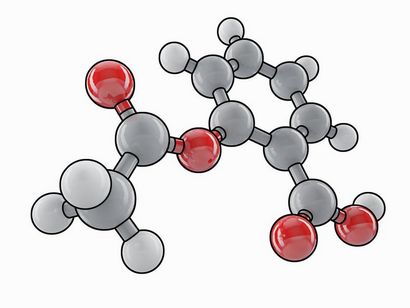
LAGUNA CONCEPTION / Getty Images
Tout d'abord, rassembler les produits chimiques et l'équipement utilisés pour synthétiser l'aspirine:
Aspirine Matériaux de synthèse
- 3,0 g d'acide salicylique
- 6 ml d'anhydride acétique *
- 5-8 gouttes de 85% d'acide phosphorique ou de l'acide sulfurique concentré *
- l'eau distillée (environ 50 ml)
- 10 ml d'éthanol
- 1% de chlorure de fer III (en option, pour tester la pureté)
* Soyez très prudent lors de la manipulation de ces produits chimiques. l'acide phosphorique ou l'acide sulfurique et l'anhydride acétique peuvent provoquer des brûlures graves.
- Papier filtre (12,5 cm)
- Bague stand avec entonnoir
- Deux 400 ml béchers
- erlenmeyer de 125 mL
- Burette de 50 ml ou de mesure de pipette
- 10 ml et 50 ml cylindre gradué
- Hotte, plaque chauffante, balance
- compte-gouttes
- tige d'agitation
- Bain de glace
- Pissette
Faisons synthétisent l'aspirine.
Continuer à 3 5 ci-dessous.
Comment faire Aspirine - Acide acétylsalicylique - Procédure

l'acide acétylsalicylique pur est blanc, mais une couleur jaunâtre est commune de légères impuretés ou de mélange avec de la caféine aspirine. Caspar Benson, Getty Images
- Peser 3,00 g d'acide salicylique et transférer dans un Erlenmeyer sec. Si vous calculera le rendement réel et théorique. assurez-vous d'enregistrer la quantité d'acide salicylique vous avez réellement mesuré.
- Ajouter 6 ml d'anhydride acétique et 5-8 gouttes de 85% d'acide phosphorique dans le ballon.
- Remuer doucement le flacon pour mélanger la solution. Placer le ballon dans un bécher d'eau chaude pour
Comment faire Aspirine - Activités
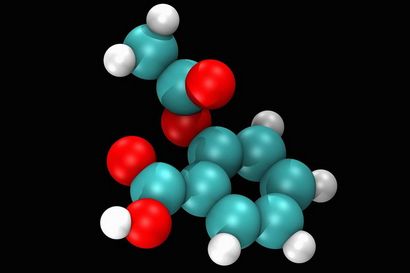
Acide acétylsalicylique ou aspirine Structure. Callista Images / Getty Images
- Vous pouvez comparer le rendement réel et théorique de l'acide acétylsalicylique en fonction de la quantité initiale d'acide salicylique. Pouvez-vous identifier le réactif limitant dans la synthèse?
- Vous pouvez comparer la qualité de l'aspirine synthétisé avec de l'aspirine commerciale et de l'acide salicylique. Ajouter une goutte de 1% de chlorure de fer III pour séparer les tubes à essai contenant quelques cristaux de chaque substance. Observer la couleur: l'aspirine pure montrerait pas de couleur, tandis que l'acide salicylique ou des traces dans l'aspirine impur montreront une couleur pourpre.
- Examiner les cristaux d'aspirine au microscope. Vous devriez voir les cristaux à petits grains blancs avec des motifs répétitifs évidents.
- Pouvez-vous identifier les groupes fonctionnels dans l'acide salicylique? Pouvez-vous prédire comment ces groupes affectent les propriétés de la molécule et comment le corps réagit à lui? L'acide salicylique a un groupe -OH (un alcool) et un groupe carboxyle -COOH (acide organique). La partie acide de la molécule est un des facteurs qui provoque une irritation de l'estomac. En plus de l'irritation causée par l'acidité, l'aspirine provoque une irritation de l'estomac en inhibant la production de prostaglandines, hormones responsables de ralentir la production d'acide gastrique.
Voici quelques questions de suivi.
Continuez à 5 sur 5 ci-dessous.
Comment faire Aspirine - Acide acétylsalicylique - Plus de questions de suivi
Les comprimés d'aspirine contiennent de l'acide acétylsalicylique et un liant. Parfois, les pilules comprennent également un tampon. Jonathan Nourok, Getty Images
Voici quelques questions supplémentaires relatives à la synthèse de l'aspirine:
- Pouvez-vous expliquer ce qui est arrivé au groupe -OH dans l'acide salicylique lorsque l'acide acétique a été ajouté? Le groupe -OH de l'acide salicylique combiné avec l'acide acétique, la production d'eau et un groupe ester. Pouvez-vous voir quel effet cela a sur le produit final? Cela a réduit la force de l'acide et l'aspirine fait plus facile à ingérer.
- Pourquoi pensez-vous que l'aspirine a été lavé avec de l'eau distillée? Comment cela affecte le produit final? Comment cela affecte le rendement réel du produit? Le lavage de la aspirine éliminé la majeure partie de l'acide salicylique n'a pas réagi et l'anhydride acétique pour donner un produit plus pur. Certains produits a été dissous et perdu dans le processus de lavage. L'eau froide a été utilisé pour réduire au minimum la dissolution du produit.