Compositions de densité et le pourcentage - LibreTexts de chimie
introduction
Densité (\ (\ rho \)) est une propriété physique trouvé en divisant la masse d'un objet par son volume. Quelle que soit la taille de l'échantillon, la densité est toujours constante. Par exemple, la densité d'un échantillon pur de tungstène est toujours 19,25 grammes par centimètre cube. Cela signifie que si vous avez un gramme ou un kilogramme de l'échantillon, la densité ne sera jamais varier. L'équation est comme suit:
Masse concerne la quantité de matière dans un objet. L'unité SI de masse est le kilogramme (kg), bien que grammes (g) sont couramment utilisés dans le laboratoire pour mesurer des quantités plus petites. Souvent, les gens confondent poids pour la masse. Poids concerne la force exercée sur un objet en fonction de la masse et de la gravité. Cela peut être écrit
Par conséquent, le poids change en raison de variations de la pesanteur et de l'accélération. Par exemple, la masse d'un cube de 1 kg continuera d'être 1 kg si elle est au sommet d'une montagne, le fond de la mer, ou sur la lune, mais son poids sera différent. Une autre différence importante entre la masse et le poids est de savoir comment ils sont mesurés. Le poids est mesuré à l'aide d'une échelle, alors que la masse doit être mesurée à l'aide d'un équilibre. Tout comme les gens confondent la masse et le poids, ils confondent aussi des échelles et des soldes. Un équilibre contrecarre les effets de la gravité tout à l'échelle incorpore. Il existe deux types de soldes trouvés dans le laboratoire: électronique et manuel. Avec un équilibre manuel, vous trouverez la masse d'un objet inconnu en ajustant ou en comparant les masses connues jusqu'à ce que l'équilibre soit atteint.
Volume décrit la quantité d'espace en trois dimensions de l'objet occupe. L'unité SI de volume est mètres cubes (m 3), mais millilitres (ml), en centimètres cubes (cm 3), et en litres (L) sont plus fréquentes dans le laboratoire. Il y a beaucoup d'équations pour trouver le volume. Voici quelques-unes des plus faciles:
Volume = (longueur) 3 ou (longueur) (largeur) (hauteur) ou (zone de base) (la hauteur)
Densité: une nouvelle enquête
Nous savons que tous les composants de densité, donc nous allons jeter un coup d'oeil de plus près la densité elle-même. L'appareil le plus largement utilisé pour exprimer la densité est g / cm 3 ou g / ml, bien que l'unité de mesure de la masse volumique est techniquement kg / m 3. grammes par centimètre cubes est équivalente en grammes par millilitre (g / cm 3 = g / ml ). Pour résoudre la densité, il suffit de suivre l'équation d = m / v. Par exemple, si vous aviez un cube métallique avec une masse de 7,0 g et le volume 5,0 cm 3. la densité serait
, Vous avez parfois besoin de convertir des unités pour obtenir les bonnes unités de densité, comme mg à g ou en 3 à 3 cm.
La densité peut être utilisée pour aider à identifier un élément inconnu. Bien sûr, vous devez connaître la densité d'un élément par rapport à d'autres éléments. Ci-dessous est un tableau de la densité de quelques éléments de la table périodique dans les conditions normales de température et de pression, ou de STP correspondant à une température de 273 K (0 ° C) et 1 atmosphère de pression.
Nom de l'élément et le symbole
Comme on peut le voir dans le tableau, l'élément le plus dense est d'osmium (Os) avec une densité de 22,6 g / cm 3. L'élément le moins dense est hydrogène (H) avec une densité de 0,09 g / cm 3.
Densité et température
Tableau \ (\ PageIndex \): Masse volumique de l'eau en fonction de la température
Même si la règle de la densité et la température a ses exceptions, il est toujours utile. Par exemple, il explique comment les ballons à air chaud fonctionnent.
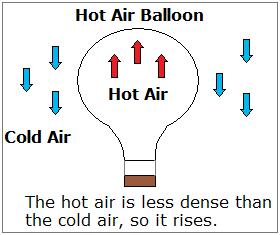
Densité et pression

Le savant grec Archimède a fait une découverte importante en 212 av. J.-C. L'histoire raconte qu'Archimède a demandé de savoir pour le roi si son orfèvre lui a triché en remplaçant son or pour la couronne avec de l'argent, un métal moins cher. Archimedes ne savait pas comment trouver le volume d'un objet de forme irrégulière, comme la couronne, alors qu'il savait qu'il pouvait distinguer entre les éléments de leur densité. En méditant sur ce casse-tête dans un bain, Archimedes a reconnu que quand il est entré dans le bain, l'eau de rose. puis il se rendit compte qu'il pouvait utiliser un processus similaire pour déterminer la densité de la couronne! Il a ensuite couru soi-disant dans les rues en criant nu « Eureka », ce qui veut dire « je l'ai trouvé! » en latin.
Archimedes ensuite testé la couronne du roi en prenant une véritable couronne d'or de masse égale et en comparant les densités des deux. La couronne du roi déplacé plus d'eau que la couronne d'or de la même masse, ce qui signifie que la couronne du roi avait un plus grand volume et a donc une densité plus faible que la vraie couronne d'or. couronne « or » du roi, par conséquent, n'a pas été faite d'or pur. Bien sûr, ce récit est contesté aujourd'hui parce que Archimedes n'a pas été précis dans toutes ses mesures, ce qui rendrait difficile de déterminer avec précision les différences entre les deux couronnes.
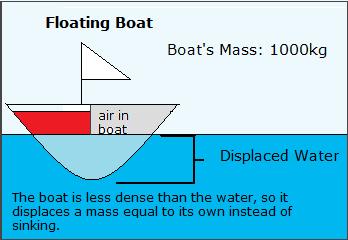
Le principe d'Archimède stipule que si un objet a une plus grande densité que le liquide qui est placé dans, il va couler et de déplacer un volume de liquide égal au sien. Si elle a une plus petite densité, il va flotter et déplacer une masse de liquide égale à lui-même. Si la densité est égale, il ne sera pas couler ou flotter. Ce principe explique aussi pourquoi des ballons remplis d'hélium avec flotteur. Ballons, comme nous l'avons appris dans la section concernant la densité et la température, le flotteur, car ils sont moins denses que l'air environnant. L'hélium est moins dense que l'air atmosphérique, de sorte qu'il se lève. Principe d'Archimède peut également être utilisé pour expliquer pourquoi les bateaux flottent. Bateaux, y compris tout l'espace aérien, dans leurs coques, sont beaucoup moins denses que l'eau. Les bateaux en acier peuvent flotter parce qu'ils déplacent leur masse dans l'eau sans submergeant tout le chemin.
Tableau \ (\ PageIndex \) ci-dessous donne les densités de quelques liquides pour mettre les choses en perspective.
Composition Pourcentage
Étapes pour le calcul de la composition pour cent des éléments d'un composé
- Trouver la masse molaire de tous les éléments dans le composé en grammes par mole.
- Trouver la masse moléculaire du composé entier.
- Diviser la masse molaire du composant de l'ensemble de la masse moléculaire.
- Vous avez maintenant un nombre compris entre 0 et 1. Multiplier par 100% pour obtenir la composition pour cent.
Conseils pour résoudre:
- La composition pour cent de tous les éléments d'un composé doit être égale à 100%. Dans un composé binaire, vous pouvez trouver le% du premier élément, puis faire 100% - (% premier élément) pour obtenir (% deuxième élément)
- Si vous utilisez une calculatrice, vous pouvez stocker la masse molaire globale à une variable telle que « A ». Cela permettra d'accélérer les calculs, et réduire les erreurs.
Exemple \ (\ PageIndex \): pentachlorure de phosphore
Quelle est la composition pour cent de phosphore et de chlore dans \ (PCl_5 \)?
Trouver la masse molaire de tous les éléments dans le composé en grammes par mole.
Trouver la masse moléculaire du composé entier.
- \ (PCl_5 \) \ (1 \ 30,975 fois \, g / mole + 5 \ times 35,453 \, g / mol = 208,239 \, g / mol \)
Diviser la masse molaire du composant de l'ensemble de la masse moléculaire.
Par conséquent, \ (PCl_5 \) est le phosphore 14,87% et 85,13% de chlore en masse.
Exemple \ (\ PageIndex \): HCl
Quelle est la composition pour cent de chaque élément dans de l'acide chlorhydrique (HCl).
trouver d'abord la masse molaire de l'hydrogène.
Maintenant, trouver la masse moléculaire de la molécule HCl:
\ [1,00794 \, g + 35,4527 \, g = 36,46064 \ g \]
Suivez les étapes 3 et 4:
Maintenant soustrayez juste pour trouver le pour cent en masse de chlore dans le composé:
Par conséquent, \ (HCl \) est 2,76% d'hydrogène et 97,24% de chlore en masse.
Composition en pourcentage dans la vie quotidienne
Les étiquettes de nutrition

Penny: The Lucky Copper Coin
Le penny devrait être appelé « la pièce de monnaie cuivrés chanceux. » Le penny n'a pas été en cuivre solide depuis une partie de 1857. Après 1857, le gouvernement américain a commencé à ajouter d'autres métaux moins chers au mélange. Le penny, étant seulement un cent, est littéralement ne vaut pas son poids en cuivre. Les gens pourraient fondre une pièce de cuivre et de vendre le cuivre pour plus que les quelques centimes valaient. Après 1857, le nickel a été mélangé avec le cuivre plus cher. Après 1864, le denier a été en bronze. Le bronze est de 95% de cuivre et 5% de zinc et d'étain. Pendant un an, 1943, le denier avait pas de cuivre dans ce dû à la charge de la guerre mondiale. Il était juste zinc acier enduit. Après 1943 jusqu'en 1982, le denier a traversé des périodes où il était en laiton ou en bronze.

Aujourd'hui, le penny en Amérique est de 2,5% de cuivre avec 97,5% de zinc. Les couches de cuivre de l'extérieur de la penny tandis que la partie interne est du zinc. Par souci de comparaison, le penny au Canada est de 94% d'acier, 1,5% de nickel et 4,5% de cuivre.
Voici une image d'un penny rayé avant et après avoir été immergé dans du jus de citron. Le jus de citron a un pH 1,5-2,5 similaire par rapport à l'estomac humain normal après nourriture a été consommée. Temps écoulé: 36 heures.


Comme vous pouvez le voir, le cuivre est largement sain et sauf par le jus de citron. Voilà pourquoi quelques centimes faits avant 1982 avec principalement du cuivre (sauf le penny 1943) sont relativement sûrs à avaler. Les chances sont qu'ils passeraient à travers le système digestif naturellement avant tout dommage pourrait être fait. Pourtant, il est clair que le zinc a été partiellement dissous, même si elle était dans le jus de citron pour seulement une quantité limitée de temps. Par conséquent, la composition pour cent de 1982 post pennies est dangereux pour votre santé et la santé de vos animaux de compagnie en cas d'ingestion.
Composition et densité pour cent sont des concepts importants en chimie. Chacun a des composants de base, ainsi que de larges applications. Les composants de densité sont: masse et le volume, les deux qui peut être plus déroutant que au premier coup d'œil. Une application du concept de densité consiste à déterminer le volume d'une forme irrégulière en utilisant une masse connue et la densité. La détermination de la composition en pourcentage, il faut connaître la masse de l'objet entier ou molécule et la masse de ses composants. Au laboratoire, la densité peut être utilisé pour identifier un élément, tandis que la composition est utilisée pour cent pour déterminer la quantité, en masse, de chaque élément présent dans un composé chimique. Dans la vie quotidienne, la densité explique tout de la raison pour laquelle les bateaux flottent les raisons pour lesquelles les bulles d'air vont essayer d'échapper à la soude. Elle affecte même votre santé, car la densité osseuse est très important. De même, la composition pour cent est couramment utilisé pour fabriquer des aliments pour animaux et des composés tels que le bicarbonate de soude trouvé dans votre cuisine.
Problèmes de densité
Ces problèmes sont destinés à être facile au début, puis deviennent progressivement plus difficiles. Sauf indication contraire, les réponses doivent être en g / ml ou l'équivalent g / cm 3.
- Si vous avez un échantillon 2,130 ml d'acide acétique avec masse .002234 kg, ce qui est la densité?
- Calculer la densité d'un échantillon de 0,03020 L d'alcool éthylique avec une masse de 23,71002 g.
- Trouvez la densité d'un échantillon qui a un volume de 36,5 L et une masse de 10,0 kg.
- Trouvez le volume en ml d'un objet qui a une densité de 10,2 g / L et une masse de 30,0 kg.
- Calculer la masse en grammes d'un objet avec un volume de 23,5 ml et une densité de 10,0 g / L.
- Calculer la densité d'un prisme rectangulaire en métal. Les dimensions du prisme sont: 5cm par 4cm par 5cm. Le métal a une masse de 50 grammes.
- Trouvez la denstiy d'un liquide inconnu dans un bécher. La masse est 165g quand il n'y a pas de liquide du bécher. Avec le liquide inconnu, la masse totale est 309g. Le volume de l'inconnu est 125mL.
- Déterminer la masse volumique en g / L d'un inconnu avec les informations suivantes. Un bain à 55 gallons pèse 137.5lb quand il est vide et 500,0 lb lorsqu'il est rempli de l'inconnu.
- Un anneau a une masse de 5,00 g et un volume de 0,476 ml. Est-ce l'argent pur?
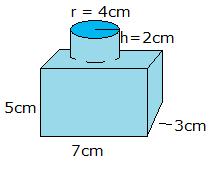
- Quelle est la densité du solide dans l'image si la masse est de 40 g? Faites votre réponse ont 3 chiffres significatifs.
11) Ci-dessous un modèle d'une pyramide trouvée à une fouille archéologique faite d'une substance inconnue. Il est trop grand pour trouver le volume en immergeant dans l'eau. En outre, les scientifiques refusent d'enlever un morceau à tester car cette pyramide est une partie de l'histoire. Sa hauteur est 150.0m. La longueur de sa base est 75.0m et la largeur est 50.0m. La masse de cette pyramide est 5.50x10 5 kg. Quelle est la densité?
Densité Problème Solutions
Problèmes de composition en pourcentage
Ces problèmes vont suivre le même schéma de difficulté que ceux de la densité.
- Calculer le pour cent en masse de chaque élément de fluorure de césium (CsF).
- Calculer le pour cent en masse de chaque élément présent dans du tétrachlorure de carbone (CCl4)
- Une solution de sel et de l'eau est un sel de 33,0% en masse et a une densité de 1,50 g / mL. Quelle est la masse du sel en grammes est en 5.00L de cette solution?
- Une solution d'eau et de HCl contenant 25% en masse de HCl. La densité de la solution est de 1,05 g / ml. Si vous avez besoin 1.7g de HCl pour une réaction, ce volume de cette solution utiliserez-vous?
- Une solution contenant 42% de NaOH en masse a une masse volumique de 1,30 g / mL. Quelle est la masse, en kilogrammes, de NaOH est à 6,00 L de cette solution?
Composition pour cent Solutions Problème
- CsF est de 87,5% de Cs et 12,5% en masse F
- CCl4 est 92,2% de Cl et 7,8% de C en masse
- 2480g
- 6,5 ml
- 2,38 kg
Les références
Tate, "Découvertes de Archimedes: A Closer Look." J.
- Il n'y a pas d'articles recommandés.
