En comparant les réactions SN1 E1 et
Imaginez que vous commencez avec l'alcool à gauche et vous souhaitez obtenir la alcènes à droite.
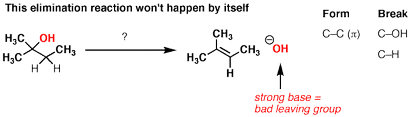
Quels sont les liens sont formés et brisés ici? Nous la formation C-C (π), nous cassons C-H, et nous cassons C-OH. Il est une réaction d'élimination.
Cela signifie que la réaction, comme il est écrit, est très peu probable.
Pourtant, il y a quelque chose de très simple que nous pouvons faire pour faire ce travail de réaction. Nous avions besoin d'avoir un meilleur groupe partant (une base plus faible). Comment peut-on le faire?
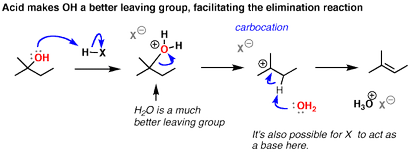
Si l'on ajoute un acide fort, on tourne OH dans H2 O +. l'acide conjugué est un groupe partant mieux. Maintenant, l'eau peut partir, la formation d'un carbocation; et une base peut rompre la liaison C-H, en formant l'alcène.
Notez que ceci est maintenant une réaction E1 classique. Le taux va dépendre de la stabilité du carbocation. Celui-ci est supérieur, il devrait donc procéder à un taux relativement élevé.
Une question se pose ici. Qu'est-ce qui va agir comme base? À l'heure actuelle, une liaison C-H adjacent à un carbocation a une acidité extrêmement élevée (au moins au-dessous de -2, si on suit pKa). Cela signifie que à peu près toute base faible (de l'eau, ou la base conjuguée de l'acide) est suffisante pour déprotoner l'atome de carbone. Il est possible que plus d'une espèce peut servir de base ici. Je l'ai montré l'eau en enlevant le proton, mais ce n'est pas déraisonnable de montrer la base conjuguée de l'acide retrait du proton dans la plupart des cas.
Maintenant vient l'une des choses sur la chimie organique qui provoque souvent des difficultés pour les étudiants. Pour une des premières fois dans nos discussions, nous avons affaire à une situation où l'on peut avoir des réactions concurrentes.
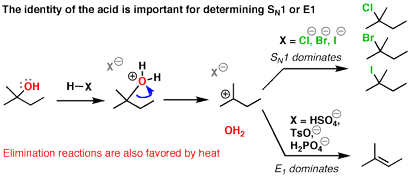
Si vous souhaitez SN1 prédominer sur E1, choisissez un acide comme HCl, HBr ou HI.
Nous avons presque fini de parler des réactions d'élimination. prochain article - nous allons parler de réarrangements.
Article suivant: La réaction E1 Avec réarrangements