Isotopes de l'hydrogène
Propriétés des isotopes de l'hydrogène
L'hydrogène a trois isotopes naturels: 1 H (protium), 2 H (deutérium), et 3 H (tritium). D'autres noyaux très instables (4 H à 7 H) ont été synthétisés en laboratoire, mais ne se produit pas dans la nature. Le radio-isotope le plus stable de l'hydrogène est le tritium, avec une demi-vie de 12,32 ans. Tous les isotopes plus lourds sont synthétiques et ont une demi-vie inférieure à une zeptosecond (10 -21 sec). Parmi ceux-ci, 5 H est le plus stable et le moins isotope stable est H 7.
Protium, l'isotope le plus commun de l'hydrogène, constitué d'un proton et un électron. Unique parmi tous les isotopes stables, il n'a pas neutrons.
1 H est l'isotope de l'hydrogène le plus commun, avec une abondance de plus de 99,98%. Le noyau de cet isotope est constitué d'un seul proton (numéro atomique = nombre de masse = 1) et sa masse est de 1,007825 amu. L'hydrogène est généralement trouvé en tant que gaz hydrogène diatomique H2. ou il se combine avec d'autres atomes dans les composés hydrogène -monoatomic est rare. La liaison H-H est l'une des liaisons plus fortes dans la nature, avec une enthalpie de dissociation de la liaison de 435,88 kJ / mol à 298 K. Par conséquent, H2 se dissocie pour seulement une faible mesure jusqu'à ce que des températures plus élevées sont atteintes. A 3000K, le degré de dissociation est seulement 7,85%. Les atomes d'hydrogène sont tellement réactifs qu'ils se combinent avec presque tous les éléments.
2 H ou deutérium (D), est un autre isotope stable de l'hydrogène. Il a une abondance naturelle de
L'utilisation la plus courante pour deuterium est en spectroscopie de résonance magnétique nucléaire. Comme résonance magnétique nucléaire (RMN) des composés d'intérêt nécessite d'être dissous dans la solution. le signal de la solution ne doit pas inscrire dans l'analyse. Comme RMN analyse les spins nucléaires des atomes d'hydrogène, l'autre propriété de spin nucléaire du deutérium est pas « vu » par l'instrument de RMN, ce qui rend les solvants deutérés hautement souhaitable en raison de l'absence d'interférence de signal de solvant.
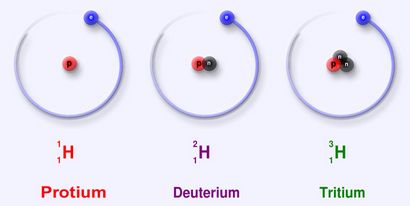
Isotopes de l'hydrogène
Les trois isotopes d'origine naturelle de l'hydrogène.